Codara Summary
Sachverhalt, Spruch und rechtliche Beurteilung – kompakt zusammengefasst.
Der Oberste Patent- und Markensenat hat durch die Präsidentin des Obersten Patent- und Markensenates Dr. Irmgard GRISS, die Räte des Obersten Patent- und Markensenates Dr. Elisabeth LOVREK und Dr. Gabriele JAGETSBERGER als rechtskundige Mitglieder und die Räte des Obersten Patent- und Markensenates Dr. Susanna SLABY und Dr. Erich TENGLER als fachtechnische Mitglieder in der Patentrechtssache der Antragstellerin S *****, Niederlande, und der ihr beigetretenen Nebenintervenientin G ***** G m b H , ***** beide vertreten durch Sonn Partner Patentanwälte, Riemergasse 14, 1010 Wien, gegen die Antragsgegnerin E *****, Großbritannien, vertreten durch die Patentanwälte Dipl.-Ing. Walter Holzer, Dr. Elisabeth Schober, Brigittenauer Lände 50, 1200 Wien, wegen Nichtigerklärung des Patentes Nr AT E 127 804, über die Berufung der Antragstellerin und ihrer Nebenintervenientin gegen die Endentscheidung der Nichtigkeitsabteilung des Österreichischen Patentamtes vom 24. Feber 2010, N 15/2007-13, entschieden:
Der Berufung der Antragstellerin und ihrer Nebenintervenientin wird nicht Folge gegeben.
Die Antragstellerin und ihre Nebenintervenientin sind schuldig, der Antragsgegnerin die mit EUR 2.994,09 bestimmten Kosten (darin enthalten EUR 499,01 Umsatzsteuer) des Verfahrens binnen 14 Tagen zu ersetzen.
Gründe:
Die Antragsgegnerin ist Inhaberin des am 24. April 1991 unter Inanspruchnahme einer britischen Priorität vom 25. April 1990 (GB 9 009 229) angemeldeten und mit Wirkung für Österreich erteilten europäischen Patents AT E 127 804. Das Patent umfasst 22 Patentansprüche mit folgendem Wortlaut:
1. 2-Methyl-10-(4-methyl-1-piperazinyl)-4H-thieno-[2,3-b][1,5]benzodiazepin oder ein Säureadditionssalz davon.
2. 2-Methyl-10-(4-methyl-1-piperazinyl)-4H-thieno-[2,3-b][1,5]benzodiazepin oder ein pharmazeutisch brauchbares Säureadditionssalz davon.
3. 2-Methyl-10-(4-methyl-1-piperazinyl)-4H-thieno-[2,3-b][1,5]benzodiazepin.
4. Verbindung nach Anspruch 2 oder 3 zur Verwendung als Arzneimittel.
5. Verwendung einer Verbindung nach Anspruch 2 oder 3 zur Verwendung zur Herstellung eines Arzneimittels zur Behandlung einer Störung im Zentralnervensystem.
6. Verwendung einer Verbindung nach Anspruch 2 oder 3 zur Verwendung zur Herstellung eines Arzneimittels zur Behandlung von Schizophrenie.
7. Verwendung einer Verbindung nach Anspruch 2 oder 3 zur Verwendung zur Herstellung eines Arzneimittels zur Behandlung einer schizophreniformen Krankheit.
8. Verwendung einer Verbindung nach Anspruch 2 oder 3 zur Verwendung zur Herstellung eines Arzneimittels zur Behandlung von akuter Manie.
9. Verwendung einer Verbindung nach Anspruch 2 oder 3 zur Verwendung zur Herstellung eines Arzneimittels zur Behandlung von leichten Angstzuständen.
10. Pharmazeutische Zusammensetzung, umfassend eine Verbindung nach Anspruch 2, zusammen mit einem pharmazeutisch brauchbaren Verdünnungsmittel oder Träger dafür.
11. Dosiseinheitsform, umfassend 0.1 bis 20 mg einer Verbindung nach Anspruch 2.
12. Dosiseinheitsform, umfassend 0.5 bis 10 mg einer Verbindung nach Anspruch 2.
13. Pharmazeutische Zusammensetzung, umfassend eine Verbindung nach Anspruch 3, zusammen mit einem pharmazeutisch brauchbaren Verdünnungsmittel oder Träger dafür.
14. Pharmazeutische Zusammensetzung in Kapsel- oder Tablettenform, umfassend 0.1 bis 20 mg der Verbindung von Anspruch 3.
15. Pharmazeutische Zusammensetzung in Kapsel- oder Tablettenform, umfassend 0.5 bis 10 mg der Verbindung von Anspruch 3.
16. Pharmazeutische Zusammensetzung in Kapsel- oder Tablettenform, umfassend 2.5 bis 5 mg der Verbindung von Anspruch 3 zusammen mit einem pharmazeutisch brauchbaren Verdünnungsmittel oder Träger dafür.
17. Pharmazeutische Injektion, die in der Dosiseinheitsform 0.1 bis 20 mg einer Verbindung nach Anspruch 2 oder 3 umfasst.
18. Pharmazeutische Injektion, die in der Dosiseinheitsform 0.5 bis 10 mg einer Verbindung nach Anspruch 2 oder 3 umfasst.
19. Pharmazeutische Injektion nach Anspruch 17 oder 18, die eine langzeitwirkende Formulierung für intramuskuläre Injektionen ist.
20. Verfahren zur Herstellung einer Verbindung nach Anspruch 1, umfassend
(a) die Umsetzung von N-Methylpiperazin mit einer Verbindung der Formel,
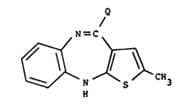
(b) den Ringschluss einer Verbindung der Formel
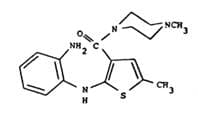
21. Verbindung der Formel,
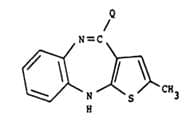
wobei Q –NH2, -OH, oder –SH ist, und wenn Q –NH2 ist, Salze davon.
22. Verbindung nach Anspruch 21, wobei Q –NH2 ist oder ein Salz davon.
Das Streitpatent betrifft die Verbindung 2-Methyl-10-(4-methyl-1-piperazinyl)-4H-thieno-[2,3-b][1,5]benzodiazepin (Beilage ./1), oder bei unterschiedlicher Nummerierung vom S-Atom beginnend 2-Methyl-4-(4-methyl-1-piperazinyl)-10H-thieno-[2,3-b][1,5]benzodiazepin zur Verwendung als Antipsychotikum (Behandlung von Schizophrenie) mit dem Namen Olanzapin mit folgender Strukturformel:
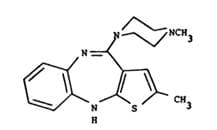
Die Patentschrift beschreibt Nebenwirkungen, die bisher verwendete Antipsychotika hervorriefen, wie etwa starke extrapyramidale Symptome (beeinträchtigte Bewegungsabläufe), die insbesondere bei Verabreichung von Haloperidol beobachtet worden seien. Aus der Gruppe der tricyclischen Antipsychotika sei Clozapin eingeführt worden, das bei einigen Patienten eine lebensbedrohliche Agranulozystose (Verringerung der weißen Blutzellen) verursacht habe. In der britischen Patentschrift GB 1 533 235 (Beilage ./3) seien Thienobenzodiazepine mit antipsychotischer Wirkung beschrieben. Die darin offenbarte Stammverbindung 7-Fluor-2-methyl-10-(4-methyl-1-piperazinyl)-4H-thieno-[2,3-b][1,5]benzodiazepin oder Flumezapin zeige in klinischen Versuchen erhöhte Werte an Creatininphosphokinase, Glutamat-Oxalacetat-Transaminase und Glutamat-Pyruvat-Transaminase.
Die Verbindung mit der oben dargestellten Strukturformel weise im Vergleich mit Flumezapin und anderen verwandten Verbindungen überraschende und exzellente Eigenschaften auf, etwa hohe Aktivität der Patienten bei überraschend niedrigen Dosierungen und gleichzeitig deutlich geringere bzw fehlende Nebenwirkungen gegenüber den Verbindungen des Standes der Technik.
Die Antragstellerin beantragt die Nichtigerklärung des Patents im Umfang aller erteilen Ansprüche. Sie bestreitet die Neuheit und eine erfinderische Tätigkeit. Zur Begründung stützt sie sich zusammengefasst auf die vorveröffentlichte Druckschrift GB 1 533 235 (Beilage ./3) als Stand der Technik.
Die Patentansprüche 1 bis 9 sowie 20 bis 22 seien durch die vorveröffentlichte Druckschrift J. Med. Chem. 23 (1980) 878-884 (Beilage ./5) vorweggenommen. Die auf pharmazeutische Zusammensetzungen, Dosiseinheitsformen sowie Verabreichungsformen (Injektionen) gerichteten Patentansprüche 10 bis 19 beruhten gegenüber Beilage ./5 unter Berücksichtigung von Beilage ./3 nicht auf einer erfinderischen Tätigkeit.
Die Autoren in der peer-reviewed Zeitschrift „Pharmazie“ hätten sich bereits vor dem Prioritätszeitpunkt des Streitpatents mit der antipsychotischen Wirkung von 4-Piperazinyl-10H-thienodiazepinen befasst. Eine allgemeine Strukturformel werde in der Tabelle 1 der Beilage ./7 gezeigt:
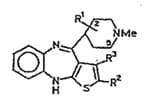
Einem organischen Chemiker fiele bei Betrachtung dieser Strukturformel sofort auf, dass der gebundene Heterozyklus nicht mit dem Titel der Veröffentlichung übereinstimme. Laut der Strukturformel sei ein Piperidyl-Substituent (mit einem Stickstoff-Heteroatom) gezeigt, während laut Titel ein Piperazinyl-Substituent, also mit zwei Stickstoff-Heteroatomen, vorhanden sei. Die angegebene Nummerierung des Heterozyklus zeige einem Fachmann jedoch klar, dass der gezeichnete Heterozyklus fehlerhaft sei und lediglich ein Stickstoffatom an der Bindungsstelle zum Thienobenzodiazepin-System vergessen worden sei, um der IUPAC-Nomenklatur und Nummerierung von Heterozyklen zu entsprechen. In der Tabelle I seien nun für den Fachmann klar ersichtlich verschiedene 4-Piperazinyl-10H-thienodiazepine geoffenbart. Von besonderer Bedeutung sei dabei die Verbindung 11 mit R1 = H, R2 = Methyl, R3 = H, die zweifellos Olanzapin beschreibe. Demgemäß sei Olanzapin zum Prioritätszeitpunkt des Streitpatents (25. April 1990) bereits durch die Veröffentlichung von Schauzu et al. (1983; Beilage ./7) neuheitsschädlich vorweggenommen. Auch die antidopaminerge bzw antipsychotische Wirksamkeit und somit die Verwendung als Arzneimittel (Ansprüche 1 bis 4) sei zwingend vorweggenommen.
Insbesondere bei Zusammenschau der Beilagen ./7 und ./8 (US 4 115 574 B1) sei die Verwendung zur Herstellung eines Medikaments zur Behandlung einer Störung im Zentralnervensystem nahe gelegt. Schizophreniforme Krankheiten würden bekanntermaßen wie Schizophrenie behandelt (Beilage ./9).
Die auf Seiten der Antragstellerin dem Verfahren beigetretene Nebenintervenientin beantragt ebenfalls die gänzliche Nichtigerklärung sämtlicher Patentansprüche.
Die Antragsgegnerin beantragt die Abweisung des Antrags. Die Forschungsarbeit Beilage ./5 erwähne Olanzapin weder explizit noch implizit.
Eine Offenbarung „zwischen den Zeilen“ käme nur dann in Betracht, wenn eine „notorisch bekannte“ und vollständig identische Wirkung vorläge. Im vorliegenden Fall bestünde weder eine „notorische“ Kenntnis von Olanzapin noch eine notorische Kenntnis der Wirkung nicht getesteter Substituentenkombinationen. Hinzu käme, dass Beilage ./5 keine Grundlage für eine solche Kombination liefere, sondern nur tatsächlich getestete Stoffe und deren Versuchsergebnisse aufliste. Es sei vor dem Hintergrund des Verbots einer ex-post Betrachtung unzulässig, willkürlich einzelne Substituenten herauszulösen und zu kombinieren, um zu Olanzapin zu gelangen. Eine Markush-Formel in einer Patentschrift solle den Leser über alle möglichen Kombinationen informieren, die durch freie Wahl der Substituenten erzielt werden können. Beilage ./5 sei ein Testbericht. Der Leser werde nicht über frei kombinierbare Substituentenlisten über alle Unterkombinationen informiert. Allein die Untersuchungsergebnisse für 59 bestimmte Stoffe seien wiedergegeben. Andere Stoffe würden weder erwähnt noch hypothetisch diskutiert. Der Leser werde durch Beilage ./5 nicht angeregt, die Substituenten frei miteinander zu kombinieren.
Die Verwendungsansprüche 4 bis 9 seien ebenfalls rechtsbeständig: Eine Verwendung einer neuen Verbindung sei per se neu. Die Tierversuche seien für die Behandlung von Schizophrenie beim Menschen nicht aussagekräftig, unter anderem auch, weil Verbindung Nr 9 entgegen den Tierversuchsergebnissen erhöhte Enzymwerte sowie extrapyramidale Nebenwirkungen zeige. Beilage ./5 stelle nur erste Screening-Modelle dar, die keine Vorhersagen auf das Verhalten der getesteten Substanzen beim Menschen erlaubten und beschränke sich auf eine kleine Auswahl gestesteter Verbindungen als Ausgangspunkt für weitere Tests und weitere notwendige Erprobungen.
Die Patentansprüche 20 bis 22 bezögen sich auf die Herstellung der erfindungsgemäßen Verbindung und seien nicht expressis verbis in der Beilage ./5 offenbart.
Auch in Beilage ./7 sei Olanzapin nicht neuheitsschädlich offenbart. Einer fehlerhaften Darstellung in einer Druckschrift, die der Durchschnittsfachmann ohne Weiteres erkenne und richtig stelle, sei kein Offenbarungsgehalt beizumessen. Maßgeblich sei der wahre Gehalt einer Druckschrift, wie er sich dem Fachmann ohne Weiteres erschließe. Die selektiv durchgeführten Korrekturen der Antragstellerin erfolgten in rückschauender Betrachtung, seien praxisfern, naturwissenschaftlich unzutreffend und widersprächen der fachmännischen Arbeitsweise. Eine Free-Wilson Analyse sei ein mathematisches Verfahren und benötige immer ein „Trainingsset“ experimenteller Ergebnisse. Beilage ./7 vergleiche experimentelle Daten mit rechnerisch ermittelten Daten. Die Angaben in Beilage ./7 seien offensichtlich widersprüchlich, da der Titel nicht mit der Strukturformel übereinstimme. Der Fachmann könne dem Titel oder der Formel folgen. Beide Alternativen seien für den Fachmann theoretisch möglich und sinnvoll. Der Fachmann würde den Widerspruch dahin auflösen, dass er die einzig zitierte Referenzarbeit in der Fußnote zu Rate ziehe. Die zitierte Arbeit (Beilage ./D) löse den Widerspruch ohne Weiteres auf. Der Fachmann erkenne unmittelbar, dass die Formel sogar zwei Fehler aufweise. Der Widerspruch in Beilage ./7 sei daher im Sinne von Piperazinyl-Verbindungen mit einer Fluorsubstitution aufzulösen. Die vermeintlich neuheitsschädlich dargestellte Verbindung Nr 11 der Tabelle sei daher nichts anderes als die bereits bekannte Verbindung Flumezapin .
Beilage ./8 zeige eine „Continuation Application“ des US-Äquivalents der GB 1 533 235 (Beilage ./3) und eine Ethylflumezapin-Leitstruktur. Sie offenbare Olanzapin nicht, weshalb jedwede mögliche Information hinsichtlich therapeutischer Zwecke, Dosierung, Verabreichungsformen oder Verabreichungswege den Fachmann dennoch nicht in die Lage versetze, ohne erfinderische Tätigkeit zu den Olanzapin -umfassenden Zusammensetzungen zu gelangen.
Die Nichtigkeitsabteilung wies den Antrag ab.
Sie vertrat mit ausführlicher Begründung zusammengefasst die Auffassung, dass die Patentansprüche durch die Dokumente Beilage ./3, 5, 7 und 8 weder vorweggenommen noch nahegelegt worden seien.
Gegen diese am 29. Juni 2010 zugestellte Entscheidung erhoben die Antragstellerin und die Nebenintervenientin am letzten Tag der Berufungsfrist (30. August 2010; siehe § 54 Abs 2 PatG) eine von Patentanwalt Dr. Alge unterfertigte Berufung , die lediglich einen Antrag auf Abänderung der Entscheidung der Nichtigkeitsabteilung samt Kostenverzeichnis und einen Verweis auf eine dem Schriftsatz angeschlossene Berufungsbegründung enthielt.
Da eine Berufungsbegründung im Schriftsatz tatsächlich fehlte, erteilte die Nichtigkeitsabteilung den dem Vertreter der Antragstellerin und der Nebenintervenientin am 17. September 2010 zugestellten Auftrag, binnen zwei Wochen die Berufungsbegründung vorzulegen.
Diesem Auftrag entsprach der Vertreter der Antragstellerin am letzten Tag der Verbesserungsfrist durch Vorlage einer von Patentanwalt Dipl.-Ing. Pawloy unterfertigten Berufungsbegründung.
Die Antragsgegnerin beantragt in ihrer Berufungsbeantwortung, die Berufung zurückzuweisen; hilfsweise, ihr nicht Folge zu geben.
Die Berufung ist nicht berechtigt.
1. Gemäß § 138 Abs 3 S 2 PatG hat die Berufung einen begründeten Berufungsantrag zu enthalten. § 139 Abs 2 PatG sieht in Anlehnung an § 474 Abs 2 ZPO iVm §§ 84, 85 ZPO ein Verbesserungsverfahren für rechtzeitig überreichte Berufungen vor, die einen – auch inhaltlichen – Mangel aufweisen. Wird allerdings eine Berufung bewusst nicht begründet, sondern etwa schon bei Einbringung der Berufung eine Frist für das Nachreichen der Begründung beantragt, so leidet die Berufung an keinem Mangel, der nur versehentlich oder durch Unkenntnis der gesetzlichen Vorschriften unterlaufen wäre. Ein verbesserungsfähiger Mangel liegt dann nicht vor (OPM Op 1/10 PBl 2010, 162).
Der Antragsgegnerin ist zuzugestehen, dass die Vorgangsweise der Rechtsmittelwerberinnen (Verweis auf eine separate „Berufungsbegründung“, die nicht angeschlossen war und am letzten Tag der von der Nichtigkeitsabteilung unüblich großzügig bemessenen Verbesserungsfrist vorgelegt wurde, wobei Berufung und Begründung von verschiedenen Personen unterfertigt wurden) durchaus Zweifel daran erweckt, dass das Fehlen der Begründung im ursprünglichen Schriftsatz auf einem bloßen Versehen beruhte. Die Begründung des Vertreters der Antragstellerin in der mündlichen Berufungsverhandlung (Verfassung der Begründung durch ihn; Unterfertigung des Berufungsantrags durch Dr. Alge während seiner urlaubsbedingter Abwesenheit; versehentliche Unterlassung, bereits verfasste Begründung anzuschließen) ist jedoch nicht mit Sicherheit zu widerlegen. Im Zweifel ist von einem bloßen Versehen auszugehen. Die Berufung ist daher inhaltlich zu behandeln.
2. Im Vordergrund der Berufungsausführungen steht die Behauptung der mangelnden Neuheit des Streitpatents gegenüber Beilage ./7 (G.H. Schauzu und P.P. Mager), einer Free-Wilson Analyse, die ein mathematischen Verfahren zur Aufarbeitung von Daten, nicht aber die experimentelle Ermittlung von Daten, behandelt.
2.1 Vorauszuschicken ist, dass sich die Antragstellerin in ihrem Nichtigkeitsantrag nur auf die mangelnde Neuheit der Ansprüche 1 - 4 gegenüber Beilage ./7 stützte. Auf die erstmals in der Berufung vorgebrachte mangelnde Neuheit auch der Unteransprüche 5-22 – die vor der Nichtigkeitsabteilung nur im Hinblick auf Beilage ./5 behauptet wurde – gegenüber Beilage ./7 ist daher nicht einzugehen.
2.2 Die Beurteilung, ob der Gegenstand eines Patents durch eine Vorveröffentlichung neuheitsschädlich vorweggenommen ist, erfordert die Ermittlung des Gesamtinhalts der Vorveröffentlichung. Maßgeblich ist, welche technische Information dem Fachmann klar und eindeutig ( Weiser , Patentgesetz Gebrauchsmustergesetz [2005] 110 mN zur Rsp des Patentamts) offenbart wird (4 Ob 214/04f –
2.3 Von diesen Grundsätzen ausgehend hat die Nichtigkeitsabteilung zutreffend die Neuheitsschädlichkeit von Beilage ./7 gegenüber den Patentansprüchen 1-4 verneint:
2.3.1 Beilage ./7 untersucht den Einfluss von unterschiedlichen Substituenten bei Thienobenzazepinen auf ihre antipsychotische Wirkung. Unter dem Titel „A Free-Wilson Study of 4-Piperazinyl-10H-thienobenzodiazepine Analogues“ werden gemessene und berechnete Dopinamin-Rezeptor-Bindungs-daten von Benzodiazepinen verglichen. Diese Dopinamin-Rezeptor-Bin-dungsdaten korrelieren mit der antipsychotischen Aktivität und extrapyramidalen Nebenwirkungen und wurden von 12 Verbindungen in Referenz zu Clozapin und Haloperidol gemessen. Die Daten werden in Tabellenform mit einer Strukturformel präsentiert:
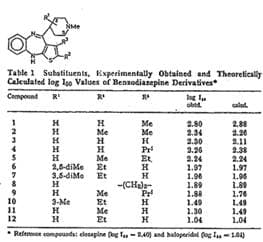
2.3.2 In Beilage ./7 stimmt der Name der Verbindungen, der im Titel genannt wird, nicht mit der allgemeinen Formel überein. Der Titel nennt 4- Piperazinyl -10H-thienobenzodiazepin-Analoga, die in der chemischen Formel dargestellten Verbindungen sind jedoch Piperidinyl -Verbindungen. Durch diesen Widerspruch zwischen Strukturformel und Titel der Arbeit ist nicht klar, welche Art von Verbindungen tatsächlich gemeint ist. Beilage ./7 liefert keine weiteren Informationen, wie beispielsweise Herstellungsverfahren der Verbindungen oder Namen der einzelnen Verbindungen, die eindeutige Hinweise darauf geben könnten, ob nun Piperazinyl- oder Piperidinyl-Verbindungen vorliegen. Aus chemischer Sicht sind beide Varianten möglich.
2.3.3 Der Fachmann ist daher nicht in der Lage, ausschließlich in Kenntnis der Beilage ./7 diesen offensichtlichen Widerspruch aufzuklären. Er wird daher, um Klarheit über die tatsächlich gemeinten Verbindungen zu erhalten, die in Beilage ./7 genannte Sekundärliteratur zu Rate ziehen (Artikel im Journal of Medical Chemistry, Volume 25, 1133-1140 aus 1982 von Chakrabarti et al – Beilage ./D).
Beilage ./D zeigt auf Seite 1135 ebenso eine Strukturformel und die zugehörigen Substituenten in Tabellenform und somit 12 einzelne Verbindungen, sowie als Referenz Clozapin , Haloperidol und Hyoscin und die dazugehörigen IC50 Werte. In Beilage ./7 werden die logIC50-Werte verwendet. Bei Berechnung des Logarithmus ist sofort erkennbar, dass die in Beilage ./7 verwendeten experimentellen Daten aus Beilage ./D stammen. Auch wenn die Identität der IC50 Werte mit den logIC50-Werten nicht auf einen Blick ersichtlich ist, so ist die Berechnung des dekadischen Logarithmus für den Fachmann eine Selbstverständlichkeit. Das Arbeiten mit dekadischen Logarithmen ist eine gängige Methode, um sehr große oder sehr kleine Zahlen in ein übersichtliches Format zu bringen. Das bekannteste Beispiel dafür ist der pH-Wert von Lösungen, der der negative dekadische Logarithmus der Wasserstoffionenkonzentration ist.
Es ist auch keineswegs notwendig, dass der Fehler bei Heranziehung von Beilage ./D sofort auf den ersten Blick korrigiert werden kann. Wesentlich ist vielmehr, dass der Fachmann unter Heranziehung der Sekundärliteratur in der Lage ist, den Fehler zu korrigieren. Da der Fachmann an der technischen Realität interessiert ist, wird er das Dokument genau prüfen und nicht – wie von den Berufungswerberinnen behauptet – nur einen ersten Blick auf das entsprechende Dokument werfen.
2.3.4 Aus Beilage ./D ist – durch einfaches Umordnen der Verbindungen und Berechnen von Logarithmen – eindeutig ersichtlich, dass die Autoren von Beilage ./7 die experimentellen Dopinamin-Rezeptor-Bindungsdaten von Benzodiazepinen aus Beilage ./D übernommen haben.
Ferner ist eindeutig ersichtlich, dass insbesondere die Verbindung Nr 11 in der Beilage ./7 den getesteten Verbindungen und insbesondere der Verbindung Nr 2 der Beilage ./D entspricht, dass aber offensichtlich die Strukturformel der Beilage ./7 zwei Fehler enthält.

Formel von Tabelle I (Beilage ./D) Formel von Tabelle 1 (Beilage ./7)
Einerseits fehlt ein Stickstoffatom im Piperazinylring, andererseits die Halogenierung des Phenylrings, nämlich die Fluorierung an Position 7.
2.3.5 Aus fachmännischer Sicht ergibt sich somit, dass die fehlerhafte Strukturformel in Beilage ./7 in Übereinstimmung mit der Strukturformel der Beilage ./D korrigiert werden kann, die unstrittig nicht Olanzapin, sondern das bereits bekannte Flumezapin offenbart (ebenso BPatG X ZR 89/07).
2.3.6 Diesem Ergebnis steht nicht entgegen, dass ein fachkundiger Leser auch Überlegungen dahin anstellen könnte, dass in der Formel gemäß Beilage ./7 ein Stickstoff fehle, oder er beim Vergleich zu den Referenzverbindungen annehmen könne, dass der Phenylring halogeniert sei. Das gilt auch für die in der Berufung aufgestellte Behauptung, dass die Nummerierung des Piperidinringes in der allgemeinen Formel von Beilage ./7 nicht der IUPAC-Nomenklatur entspreche und daher auf ein fehlendes Stickstoffatom hinweise. Es könnte nämlich auch die Nummerierung vertauscht worden sein, oder es könnte die IUPAC-Nomenklatur nicht beachtet worden sein und ein anderes Nummerierungssystem verwendet worden sein, das bei der Zählung vom Atom im Ring ausgeht, das diesen an den Rest der Struktur bindet. Allein schon die Vielzahl der Interpretationsmöglichkeiten schließt aus, dass der Fachmann den Fehler automatisch in dem von den Berufungswerberinnen gewünschten Sinn korrigiert. Beilage ./7 offenbart somit Olanzapin weder explizit noch implizit.
3. Erfinderischer Schritt gegenüber Beilage ./3 (GB 1 533 235) iVm Beilage ./5 (Charbati 1980)
3.1 Die Berufung kommt auf die im Nichtigkeitsantrag behauptete mangelnde Neuheit der Patentansprüche 1 bis 9 sowie 20 bis 22 gegenüber der vorveröffentlichten Druckschrift Beilage ./5 bzw Beilage ./8 nicht mehr explizit zurück, sondern stützt sich darauf, dass die Patentansprüche gegenüber Beilage ./5 unter Berücksichtigung der ebenfalls vorveröffentlichten Druckschrift Beilage ./3 als unstrittig nächstliegendem Stand der Technik nicht auf einem erfinderischen Schritt beruhten.
3.2 Die Frage der erfinderischen Tätigkeit wird nach dem vom Europäischen Patentamt herangezogenen Aufgabe – Lösungsansatz beurteilt. Im Interesse einer objektiven Beurteilung der Erfindung, die einer rückschauenden Betrachtungsweise vorbeugen soll, wird als erstes der nächstliegende Stand der Technik festgelegt, sodann die technische Aufgabe definiert und anschließend die Frage geprüft, ob die beanspruchte Erfindung angesichts des nächstliegenden Standes der Technik und der technischen Aufgabe für einen Fachmann nahe liegend gewesen wäre (OPM Op 6/08 PBl 2009, 107 mwN). Dabei ist eine Erfindung nicht schon dann nahe liegend, wenn der Fachmann aufgrund des Standes der Technik zu ihr hätte gelangen können, sondern erst, wenn er sie aufgrund eines hinreichenden Anlasses in Erwartung einer Verbesserung oder eines Vorteils auch tatsächlich vorgeschlagen hätte (17 Ob 24/09t – Nebivolol mwN).
3.3 Mit der Nichtigkeitsabteilung ist die erfinderische Tätigkeit zu bejahen:
3.3.1 Beilage ./5 offenbart eine Studie über 4-Piperazinyl-10H-thieno-[2,3-b][1,5]benzodiazepine als potenzielle Neuroleptika. Es werden die durchgeführten Experimente und die Herstellung der 4-Piperazinyl-10H-thieno-[2,3-b][1,5]benzodiazepine beschrieben, um die Struktur-Aktivitätsbeziehungen der Substituenten am Phenyl- bzw am Thiophenring zu bestimmen. Insbesondere geht es darum, die Zusammenhänge zwischen Struktur und neuroleptischer Aktivität verschiedener Substituenten zu untersuchen. Auch ein Substituent am Piperazinring wird variiert. Die Tabelle 1 aus Beilage ./5 offenbart 59 hergestellte und getestete Verbindungen sowie 6 Vergleichsverbindungen. Von diesen 59 gestesteten Verbindungen stellen die Nr 1 bis 48 spezifische 4-Piperazinyl-10H-thieno-[2,3-b][1,5]benzodiazepine dar, wobei diese eindeutig durch die Nummer der Verbindung einer Grundstruktur zuordenbar sind und deren Reste R, R1 und R2 einer spezifischen Verbindung und definierten Kombination der Substituenten entsprechen. Beim Rest R handelt es sich um niedrig substituierte und unsubstituierte Alkylgruppen oder niedrige Alkohol- oder Estergruppen. R1 steht bei den meisten getesteten Verbindungen für ein Halogenatom, insbesondere Fluor, bei einigen Verbindungen auch für Wasserstoff und bei einzelnen Verbindungen für methyl- oder stickstoff- und schwefelhältige Substituenten. R2 steht meist für Alkylgruppen.
3.3.2 Die Berufungswerberinnen meinen, dass der Durchschnittsfachmann starke Veranlassung habe, bei der in Beilage ./3 (Beispiel 26) und Beilage ./5 (Tabelle I) jeweils explizit offenbarten Verbindung 2-Ethyl-4-(4-methyl-1-piperazinyl)-10H-thieno-[2,3-b][1,5]benzodiazepin („ Ethyl-Olanzapin “) den Substituent in Stellung 2 des Tiophenringes „short“ zu halten, also „typically C1-6 alkyl“. Kürzer als Ethyl (C2) sei nur Methyl (C1), weshalb der Fachmann „zwanglos“ zur Strukturformel von Olanzapin gelange.
3.3.3 Die Schlussfolgerung der Antragstellerin, es liege nahe, dass Methyl – mit kürzester Kettenlänge – die höchste Aktivität entfalten werde, ist nicht nachvollziehbar, weil Methyl-, Ethyl und i-Propyl-Reste als gleichwertig aufgezählt werden. Die Auswahl von 2-Ethyl-4-(4-methyl-1-piperazinyl)-10H-thieno-[2,3-b][1,5]benzodiazepin als vielversprechendste Verbindung für die Weiterentwicklung neuer Wirkstoffe anzusehen, kann nur durch eine – im Patentrecht unzulässige – rückschauende Betrachtung erfolgen. In Beilage ./5 ist 2-Ethyl-4-(4-methyl-1-piperazinyl)-10H-thieno-[2,3-b][1,5]benzodiazepin nicht als vielversprechendste Verbindung angeführt. Vielmehr findet sich in Beilage ./5 auf Seite 879 der Hinweis: „ The substitution of the phenyl ring with a halogen atom (Cl, F) at Position 7 enhanced the activity” („Eine Substitution des Phenylrings mit einem Halogenatom (Cl, F) an der Position 7 erhöhte die Aktivität“). Das legt dem Fachmann nahe, den Phenylring mit einem Halogenatom zu substituieren. Der Fachmann wird daher eindeutig nicht zu 2-Methyl-4-(4-methyl-1-piperazinyl)-10H-thieno-[2,3-b][1,5]benzodiazepin geführt, das nicht mit einem Halogenatom substituiert ist.
3.3.4 Auch die Ausführungen in der Berufung zu Beilage ./3 (Seite 3, Zeile 8) überzeugen nicht:
Tatsächlich lautet der vollständige Satz:
„ the thiophene ring may be substituted for instance, by one or more groups selected from C1 8 alkyl, typically C1-6 alkyl, C2-4 alkenyl, C1-4 haloalkyl, C2-4 alkanoyl, nitro, halogen, and optionally substituted phenyl” („der Thiophenring kann beispielsweise substituiert sein mit einer oder mehreren Gruppen ausgewählt aus: C1 8 alkyl, typischerweise C1-6 Alkyl, C2-4 Alkenyl, C1-4 Haloalkyl, C2-4 Alkanoyl, Nitro, Halogen, und optional substitutiertem Phenyl“).
Wieso der Fachmann aus dieser großen Auswahl gerade zu Methyl als Substituenten an der Stelle 2 des Thiophenringes kommen soll, ist nicht nachvollziehbar. Auch diese Schlussfolgerung könnte nur bei einer rückschauenden Betrachtung gezogen werden. Darüber hinaus sind auf Seite 3 der Beilage ./3 bevorzugte Verbindungen angeführt - 2-Methyl-4-(4-methyl-1-piperazinyl)-10H-thieno-[2,3-b][1,5]benzodiazepin ist nicht darunter.
3.3.5 Weder Beilage ./3 noch Beilage ./5, noch eine Kombination der beiden Dokumente legen somit 2-Methyl-4-(4-methyl-1-piperazinyl)-10H-thieno-[2,3-b][1,5]benzodiazepin oder seine Säureadditionsalze nahe. Daraus folgt, dass auch sämtliche von dieser Verbindung abgeleiteten Ansprüche nicht durch die Dokumente Beilage ./3 und/oder Beilage ./5 nahe gelegt sind.
4. Auswahlerfindung aus Beilage ./3
4.1 Die Berufungswerberinnen sind der Auffassung, dass Olanzapin eine „Auswahl“ der in Beilage ./3 offenbarten Gruppe von Verbindungen sei und nur bei – nach Auffassung der Berufung nicht verwirklichter – kumulativer Erfüllung der für eine Auswahlerfindung maßgeblichen Kriterien schutzfähig sei.
4.2 Der Begriff „Auswahlerfindung“ bezeichnet die Auswahl bestimmter Bereiche aus einem bereits bekannten größeren Bereich im Sinne eines Herausgreifens eines gewisse Besonderheiten aufweisenden Beispiels, dessen herausragende Eigenschaften zuvor nicht bekannt waren. Eine Auswahlerfindung ist dann neu, wenn aus einem größeren Bereich des Standes der Technik der ausgewählte Teilbereich jedes der drei folgenden Kriterien erfüllt (OPM Op 5/05):
1. der ausgewählte Teilbereich ist im Vergleich zu dem bekannten Bereich eng,
2. der ausgewählte Teilbereich hat genügend Abstand von konkreten, im Stand der Technik offenbarten Beispielen und von den Eckwerten des bekannten Bereichs und
3. der ausgewählte Teilbereich ist kein willkürlicher Ausschnitt des Standes der Technik, dh keine bloße Ausführungsform des Standes der Technik, sondern eine andere Erfindung (gezielte Auswahl, neue technische Lehre), das Herausgreifen eines gewisse Besonderheiten aufweisenden Beispiels, dessen herausragende Eigenschaften zuvor nicht bekannt waren.
4.3 Die Auffassung, die Erfindung erfülle die Kriterien 2 und 3 nicht, teilt der OPM nicht:
4.3.1 Beilage ./3 beschreibt eine große Zahl von Benzodiazepinen mit einer Markush-Formel, unter die 2-Methyl-4-(4-methyl-1-piperazinyl)-10H-thieno-[2,3-b][1,5]benzodiazepin ( Olanzapin ) fällt. In der Beschreibung werden die Benzodiazepine zur Behandlung des Zentralnervensystems vorgeschlagen, wovon expressis verbis 71 Verbindungen genannt sind. Allein am Phenyl- und am Thiophenring des Benzodiazepineringsystem sind jeweils 2 mögliche Positionen für Substitutionen angegeben, sodass sich eine Vielzahl an "Nachbarverbindungen" ergibt. Falls man im vorliegenden Fall überhaupt vom Abstand zwischen zwei benachbarten Verbindungen sprechen kann, also geringsten Abänderungen der Substiutenten um das organisch-che-misch Nächstliegenste, wie es von der Antragstellerin beschrieben wird, kann das in einem Fall die Abänderung immer um eine Kohlenwasserstoffgruppe weniger oder mehr sein, kann innerhalb einer Hauptgruppe im Periodensystem sein, also von Fluor zu Chlor usw, wird aber spätestens bei den genannten Nitro-, Trifluormethyl-, Methylthio-, N,N-diamethylsulfonamid-, Pentyl- oder Vinyl-Gruppen schwieriger, wobei sich vor allem immer mehr Möglichkeiten ergeben.
4.3.2 Gerade bei der pharmazeutischen Verwendung von chemischen Substanzen ist im Übrigen die Wirkung bei – auch bloß geringfügigen – Änderungen an Substituenten nicht vorhersehbar. Der Austausch einer Ethyl- durch eine Methylgruppe kann die Wirksamkeit bzw das Wirksamkeitsspektrum eines Arzneimittels deutlich ändern, wie die Antragsgegnerin in der mündlichen Berufungsverhandlung am Beispiel des Arzneimittels Valium, bei welchem der Austausch einer Methylgruppe durch eine Ethylgruppe signifikanten Einfluss auf die Wirkung des Arzneimittels habe, anschaulich darlegte. Daraus folgt aber, dass auch bei strukturell sehr ähnlichen Substituenten nicht zwingend auf eine ähnliche pharmazeutische Wirkung geschlossen werden kann. Kriterium 2, also ein ausreichender Abstand von 2-Methyl-4-(4-methyl-1-piperazinyl)-10H-thieno-[2,3-b][1,5]benzodiazepin ( Olanzapin ) zu den Verbindungen der Beilage ./3, ist daher erfüllt.
4.3.3 Die unerwartete und überraschend exzellente Wirkung von 2-Methyl-4-(4-methyl-1-piperazinyl)-10H-thieno-[2,3-b][1,5]benzodiazepin ( Olanzapin ) ist im Streitpatent hervorgehoben. Die im Streitpatent näher beschriebenen Wirkungen (Eignung als potenzielles Neuroleptikum schon bei geringer Dosierung; keine extrapyramidalen Nebenwirkungen; kein Auftreten von Agranulozytose; geringeres Auftreten von erhöhten Leberenzymwerten) sind Beilage ./3 nicht zu entnehmen. Auch das dritte Kriterium für eine Auswahlerfindung, nämlich die unerwartete Wirkung von Olanzapin, ist verwirklicht.
5. Im Zusammenhang mit ihren Ausführungen zur Auswahlerfindung bezieht sich die Berufung ferner auf die von der Antragstellerin und der Nebenintervenientin mit Schriftsatz vom 23. Feber 2010 vorgelegten Urkunden Beilagen ./10 und 11. Diese Urkunden wies die Nichtigkeitsabteilung in der mündlichen Verhandlung vom 24. Feber 2010 (Seite 14 des Protokolls) zurück; die Zurückweisung blieb ungerügt. Auch in der Berufung selbst wird ein auf die Zurückweisung der Urkunden gegründeter Verfahrensmangel nicht geltend gemacht. Ein Eingehen auf die Argumente der Berufungswerberinnen zu den zurückgewiesenen Urkunden kommt daher nicht in Betracht. Das gilt auch für die auf Beilagen ./10 und 11 gestützte – neue – Behauptung, das Streitpatent sei aufgrund unzureichender bzw inkorrekter Daten erteilt worden.
6. Der Berufung war nicht Folge zu geben.
Die Entscheidung über die Kosten des Berufungsverfahrens gründet sich auf §§ 122 Abs 1 und 140 PatG iVm §§ 41, 50 ZPO und § 23 Abs 9 RATG.
Rückverweise
Keine Ergebnisse gefunden